

UB-612新冠疫苗第三劑 (追加劑 ) 臨床數據,已展現安全、廣譜的B細胞和T細胞雙重免疫力。
有關SARS-CoV-2奧米克隆變異株 (Omicrons BA.1, BA.2 和 BA.5),以及應用新冠病毒雙價疫苗做為第四針的核准和施打對象,正在全球引起關心和討論。經仔細研究和比對,聯亞生技的第一代UB-612新冠疫苗第三劑 (第一追加劑) 臨床數據,已展現安全、廣譜 (包括針對Omicrons) 的B細胞和T細胞雙重免疫力。
聯亞生技整合臨床一期和二期第三劑 (追加劑) 試驗結果,剛於8月30日刊登在臨床醫學MedRxiv (doi: https://doi.org/10.1101/2022.08.26.22279232)。由於UB-612疫苗設計兼顧棘突和非棘突蛋白(Spike and non-Spike proteins),而且除了以S1-RBD (和病毒受體ACE2結合之蛋白區段)作為激活B細胞之抗原、也以保守不會突變表位(conserved, nonmutable epitopes)的五個區段作為激活T細胞抗原,已經引起廣大迴響,並於7月26日白宮次世代新冠疫苗高峰會領銜輝瑞及莫德納疫苗,展現其前瞻性疫苗設計的廣譜效力。
SARS-CoV-2病毒因高度變異特性,幾乎每季都會出現大幅突變。台灣全民雖能在過去兩年間躲過多種變異株之侵襲,但在今年4月起已不勝抵擋Omicron病毒株,目前台灣感染人數已自一萬人驟升至目前五百多萬人。和世界其他地區一樣,Omicron病毒株尤其是BA.5變種將成為主流病毒株。現行官方核准的疫苗,在對抗各種Omicron變異株的表現又如何,值得大家一起探討。
在各家疫苗給予未曾受感染者 (infection-free persons) 施打自己的第三劑 (第一追加劑, homologous boosting)後,以「人造假病毒」病毒中和效價分析 (pseudovirus-neutralization, 50% 幾何平均值GMT, 亦即pVNT50/ID50) 的結果顯示:UB-612對BA.1/BA.2/BA.5中和效價值,均高於莫德納 (mRNA-1273)、輝瑞 (BNT162b2)、和Novavax,且遠勝過高端 (MVC-COV1901)、阿斯理康 (AZ1222)、科興 (CoronaVac) 和國藥 (BBIBIP) 疫苗 (參見表 1A)。以對抗傳染力最強的BA.5之pVNT50為例,UB-612中和效價分析可高達854,NVX-CoV2373為582,莫德納為378,輝瑞360,科興為75,阿斯理康為43。由此數據顯見,UB-612疫苗發揮B 細胞和T細胞免疫設計理念,第三劑(第一加強針)已經具備對抗目前台灣所面臨之大敵Omicron BA.5變異株。UB-612明顯遠優於AZ疫苗之結果。

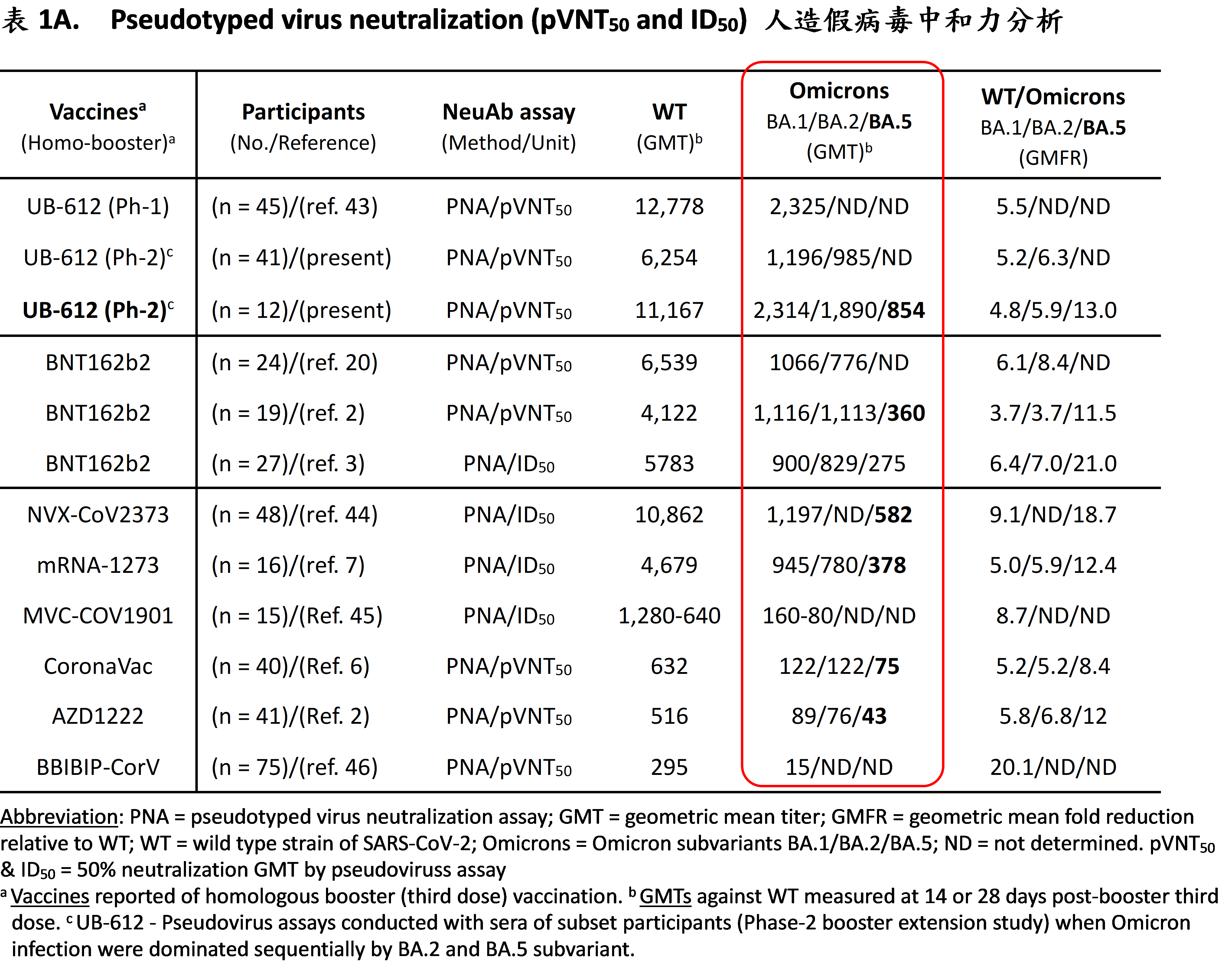
有必要在此先提醒注意,人造假病毒分析 (pseudovirus assay) 是僅以棘突蛋白 (Spike protein only) 建置的便利分析方法。然而活病毒分析 (live virus assay) 才是反映真實病毒狀況,亦即涵蓋自然存在的棘突加上非棘突本體蛋白(Spike + non-Spike proteins)。目前已知的第一代及次世代疫苗均僅以棘突蛋白作為抗原的簡易疫苗設計,當然就無能辨認病毒非棘突蛋白的本體結構。如果非棘突蛋白也發生突變,現行疫苗產生的抗體不只毫無抵抗能力、也不會引起對非棘突蛋白本體結構的 B和T 細胞的免疫記憶了。這正是目前所有僅以棘突蛋白作為抗原的疫苗無法避免之先天缺失。
因此,簡單推理,人造假病毒分析和活病毒分析法所得結果,兩者將存在著不一致性 (inconsistency),除非疫苗抗原設計同時兼顧棘突和非棘突蛋白。這可由下例活病毒測試實例,獲得驗證。
同樣,各疫苗施打自己的第三劑 (第一追加劑, homologous boosting) 後,以「活病毒」測試免疫血清中和效價 (live virus-neutralization, 50%幾何平均值GMT, 亦即VNT50/FRNT/PRNT50) 顯示,UB-612展現中和BA.1之效價遠超其他(莫德納,輝瑞,阿斯理康疫苗) 6到12倍之多 (參見表1B)。這個結果合理,因為UB-612也可辨認到病毒非棘突蛋白的保守、不會突變表位區域 (conserved, nonmutable epitopes),產生深刻的T細胞免疫記憶,進而激化B細胞免疫反應。

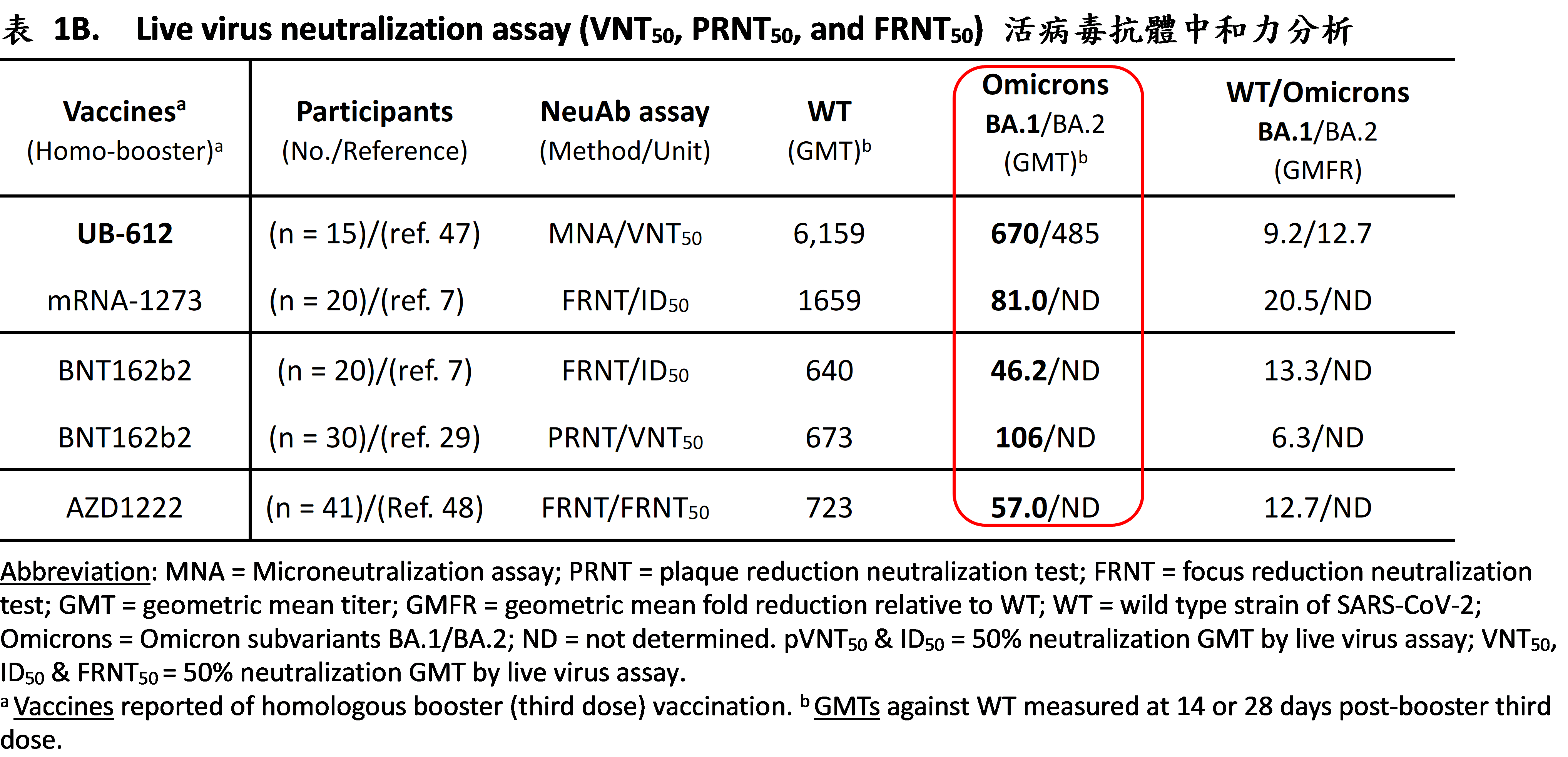
顯然,這和對抗人造假病毒之中和效價 (表1A) 存在著尖銳的不一致性。品牌疫苗的第三劑在對抗Omicrons活病毒時力有未逮,難以在免疫反應最高點產生大於100的活病毒中和BA.1效價,可以預測它們中和BA.2和BA.5活病毒的力度將更為薄弱。這些結果至少預推兩件事﹕1) 在比較各種疫苗中和效價時,活病毒測試結果才真正可靠﹔2)人造假病毒測試結果僅可供參考,用以比較只含棘突蛋白為抗原的不同疫苗廠家的抗體中和效價。在綜合相互比對之下(表1A 和 1B),UB-612疫苗在真(活)和假(人工)病毒分析結果具一致性,兩種病毒中和抗體效價分析結果顯示領先所有列舉疫苗!
為何如此?最有可能是因為,UB-612抗原兼顧棘突和非棘突蛋白所產生的B細胞和T 細胞免疫反應的加乘效果。特別注意,不只棘突蛋白有30多種突變點,Omicrons變異株之間在其非棘突本體蛋白(Envelope E, Membrane M and Nucleocapsid N)也存在著微妙、特殊的突變點 (表 2A),是目前所有以棘突蛋白為唯一抗原 (Spike-only) 的疫苗無法辨識的﹔而這意謂目前使用中所有的疫苗存在著先天的T細胞免疫缺欠,難以誘發十足T細胞免疫反應力道,進而影響到B細胞使其無法產生強大和持久的全方位免疫力。

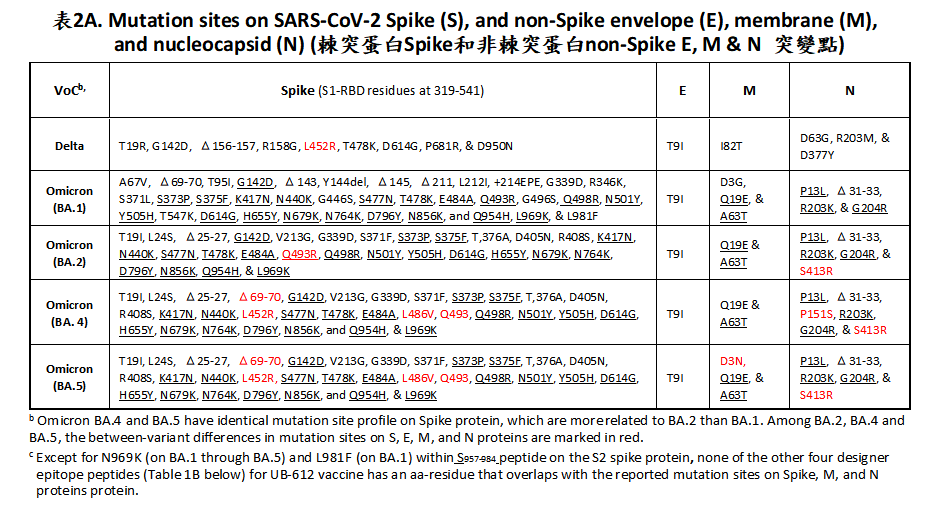
聯亞生技所開發的「精準設計型多重表位次單位疫苗UB-612」,臨床試驗數據展現出優異的功效與安全性。不同於其它次單位疫苗僅以棘突 (S) 蛋白作為唯一抗原,UB-612的組成除可誘導B細胞產生中和抗體反應的S1-RBD之外,獨創加入新冠病毒的棘突 (spike) 和非棘突蛋白 (non-spike protein) 成分,包括設計型S2x3、N及M蛋白的五個不會突變的T細胞表位區(nonmutable epitope)免疫抗原 (表 2B),這T細胞表位區已涵蓋於所有的病毒株,因此賦予UB-612的免疫廣譜性和持久性,不只可辨認Omicrons,亦可辨認未來的新突變株,具備了pan-Sarbecovirus vaccine (廣譜通用疫苗)的性質。這可同時在所有疫苗接種者活化B細胞和T細胞免疫原性,啟動全方位免疫反應,達到更完整的免疫保護作用。這五個病毒保守的表位區和宿主抗病毒干擾素Interferon-γ T細胞免疫反應以及免疫記憶的關係極為密切。
表 2B. Rationally-designed Th and CTL epitope peptides that are sequence-conserved across all VoCsa (五個保守、不會突變的表位區)

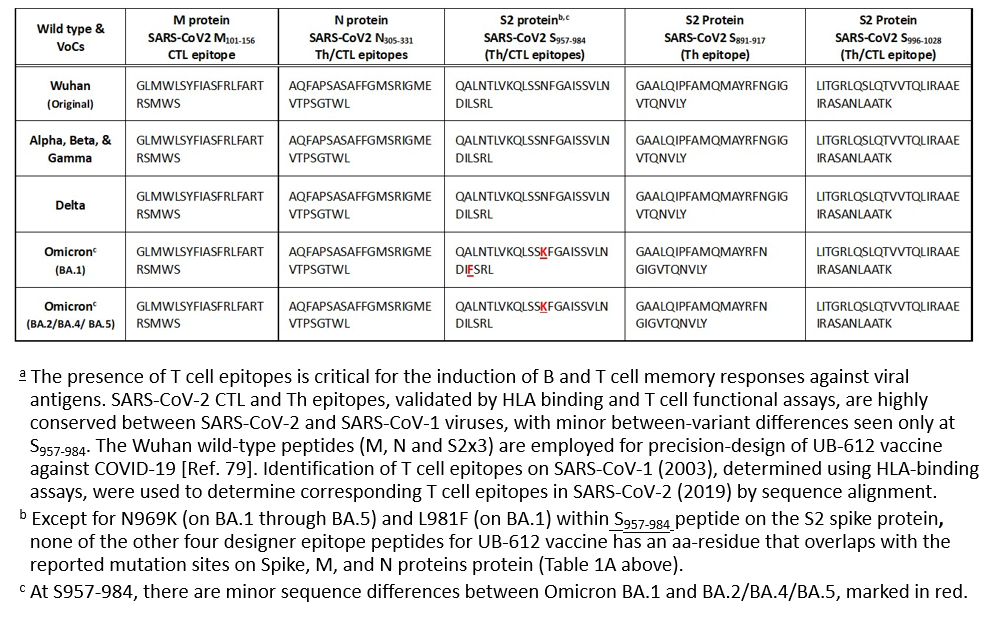
在1,480位施打兩劑或三劑UB-612疫苗的受試者中,無任何確診案例發生。此外,於今年5月國內Omicron疫情急速升溫之際,針對第二期臨床試驗受試者進行關懷電訪,接種兩劑或三劑UB-612疫苗的受試者中,初步預估保護力大於 95% (本試驗持續進行中)。
UB-612疫苗誘導之中和抗體半衰期可達187天以上,遠優於各廠牌疫苗 (表 3)。 這中和抗體長效性質已知和UB-612誘導的長效T 細胞免疫反應效力是平行一致的 (doi: https://doi.org/10.1101/2022.08.26.22279232)。
表 3. 相較於其他廠牌COVID-19疫苗,UB-612疫苗之中和抗體半衰期長,具長效疫苗保護力


目前國際上研發中或已通過EUA之COVID-19疫苗,依其設計原理、作用機轉、副作用而各有不同。T細胞免疫反應與B細胞抗體反應共同防禦病毒感染,而抗體效價會隨著時間快速消退。當前市面使用中的COVID-19疫苗已被證實無法完全抵抗新冠變種病毒感染,尤其面對棘突蛋白序列變異極大的變異株(例如:Omicron等),中和效果大為降低,無法達到最佳的預防病毒感染效果保護期短,因而民眾無奈需於短期內接種好幾劑之疫苗。
T細胞免疫可於體內維持數年。透過接種聯亞生技新冠疫苗UB-612可促使T細胞免疫記憶的產生。當經感染新冠病毒後,可誘導活化具免疫記憶的毒殺型T細胞,進而清除被病毒感染的細胞,並促進其他免疫反應,對防止病情惡化至關重要。最近一年來許多研究實證預防重症及降低死亡率之保護效果乃為T細胞免疫反應機制所然。很可惜的,AZ疫苗的設計已被證實在三劑疫苗施打時失效 (變異毒株中和力和T 細胞免疫反應力皆屬薄弱),AZ公司已宣布將淡出疫苗市場。聯亞生技自去年8月起已呼籲食藥署及評審專家將新冠疫苗之評估納入有效預防COVID-19未來可能變異株之有症狀感染、中重症或死亡預防之綜合性評估。
聯亞生技以實際臨床數據展現其UB-612除了極佳安全性外,亦在追加劑試驗中證實其優異的免疫原性與T細胞保護力,已符合疫苗開發「利大於弊」的原則。其B + T細胞免疫疫苗設計概念已受國際重視並成為未來疫苗設計之趨勢,各重要期刊均發表T細胞免疫對中重症保護力之重要性。
聯亞生技冀望食藥署、CDE與各專家委員就科學數據基礎與當前疫情趨勢審慎評估,共同為人類解決新冠病毒持續演變無止盡變異的問題,提供全球政府「清零與共存」之防疫政策另一「UB-612新利器」以達平衡點,讓UB-612投入防疫戰線,守護人民。聯亞生技將堅持先進的免疫設計原理,持續投注於未來新興傳染性疾病之疫苗開發。
有能力針對保守、不會突變的表位區 (conserved, nonmutable epitope) 而產生強大T 細胞免疫反應的疫苗,可以防阻免疫逃脫 (immune escape)1,2。同樣打第三劑追加劑,UB-612激發的T 細胞免疫力 (SFU/106 PBMC cells) 遠勝mRNA疫苗 (BNT162b2)或adeno-vectored DNA疫苗(ChAdOx1 or ADZ1222)3。追加劑前/追加劑前後之SFU單位,三劑ChAd/ChAd/ChAd 為38/45,三劑BNT/BNT/BNT 為 28/82,遠低於UB-612 在臨床二期試驗追加劑所產生的 261/374 SFU (https://doi.org/10.1101/2022.08.26.22279232)。 這和UB-612有著強大的抗BA.1活病毒中和力、而BNT162b2和ADZ1222的中和力就顯得相當微弱的結果是一致的。
目前在國內外熱烈討論的應用莫德納二價疫苗mRNA-1273.214(原始Spike加Omicron BA.1 Spike)作為第四劑(第二加強針),在未曾受感染試驗者所產生的中和 BA.5效價(人造假病毒pVNT50)為7274,比起原始mRNA-1273疫苗(第四劑)僅高出60-70%,比起第三劑mRNA-1273疫苗也僅高出90% (表1A),皆未大於2倍。這小量增加的中和BA.5效價pVNT50,是否能轉換為臨床功效有待觀察。
遺憾,莫德納公司並未於6月28日在美國FDA的審查會議裡5,呈現至關重要的「活病毒中和效價」。目前,僅知道莫德納原始疫苗mRNA-1273第三劑中和BA.1活病毒的效價 GMT (VNT50) 為81.0 (表1B),預料二價疫苗mRNA-1273.214第四劑中和BA.5活病毒效價(第二加強針的最高點,施打後第28天)只會更低。
最後,依據表1A資料整體估計,中和BA.1之效價是中和BA.2的1.3倍,是中和BA.5的 2到3倍之間。若不帶口罩、勤洗手、注意社交距離,再感染BA.5 (reinfection)或被BA.5突破感染(breakthrough infection)可能性是存在的。當然,打好打滿疫苗有其必要,而民眾是否能打到對的、好的疫苗將是一門大學問。
參考文獻:
1. S. Reynold, T cells protect against COVID-19 in absence of antibody response. NIH Research Matters. https://www.nih.gov/news-events/nih-research-matters/t-cells- protectagainst-covid-19-absence-antibody-response. June 7, 2022.
2. B. Kingstad-Bakke, et al., Vaccine-induced systemic and mucosal T cell immunity to SARSCoV-2 viral variants. PNAS. 119, e2118312119. https://doi.org/10.1073/pnas.2118312119.
3. A. P. S. Munro, et al., Safety and immunogenicity of seven COVID-19 vaccines as a third dose (booster) following two doses of ChAdOx1 nCov-19 or BNT162b2 in the UK (COVBOOST): a blinded, multicentre, randomised, controlled, phase 2 trial. Lancet. 398, 2258-2276 (2021).
4. Chalkias S, et al. A bivalent Omicron-containing booster vaccine against Covid-19. medRxiv, June 25, 2022. https://doi.org/10.1101/2022.06.24.22276703.
5. Hoge S. mRNA-1273.214 Moderna COVID-19 Investigational Bivalent Vaccine (Original + Omicron). https://www.fda.gov/media/159492/download.
關於UB-612完整論文請參閱以下國際期刊網站:
1. Wang CY, et al. UB-612 Multitope Vaccine Targeting SARS-CoV-2 Spike and Non-Spike Proteins Provides Broad and Durable Immune Responses. MedRxiv 2022.08.26.22279232; doi: https://doi.org/10.1101/2022.08.26.22279232
2. Wang CY, et al. UB-612, a Multitope Universal Vaccine Eliciting a Balanced B and T Cell Immunity against SARS-CoV-2 Variants of Concern. MedRxiv 2022.04.11.22272364; doi: https://doi.org/10.1101/2022.04.11.22272364
3. Wang CY, et al. A multitope SARS-CoV-2 vaccine provides long-lasting B cell and T cell immunity against Delta and Omicron variants. J Clin Invest. 2022 May 16;132(10):e157707. doi: 10.1172/JCI157707. PMID: 35316221; PMCID: PMC9106357.
(https://www.jci.org/articles/view/157707)
4. Guirakhoo F,….Wang CY. High Neutralizing Antibody Levels Against Severe Acute Respiratory Syndrome Coronavirus 2 Omicron BA.1 and BA.2 After UB-612 Vaccine Booster J Infect Dis. 2022 Jun 20:jiac241. doi: 10.1093/infdis/jiac241. Epub ahead of print. PMID: 35723969; PMCID: PMC9278180.
(https://academic.oup.com/jid/advance-article/doi/10.1093/infdis/jiac241/6611838)
關於UB-612 多重表位精準設計型廣譜新冠疫苗更多詳細介紹,請參考觀看以下精華影片:
1. Essential version- UB-612, a Multitope Universal Vaccine Eliciting a Balanced B and T Cell Immunity: ► 點我觀看 (英文)
2. 全球首創精準設計之廣譜新冠疫苗UB-612,優異臨床數據獲國際權威期刊《臨床研究期刊》肯定: ► 點我觀看 (中文)
3. 理想的新冠疫苗應該具備哪些特性與優勢: ► 點我觀看-上集 及 ► 點我觀看-下集 (中文)
關於UB-612
1. 可誘導中和抗體產生對抗Delta / Omicron等變異株
2. 中和抗體力價持續時間久(UB-612半衰期大於187天)
3. 可有效誘導T細胞免疫反應產生Th1傾向的細胞激素(cytokines)以對抗病毒
4. 可有效誘導免疫記憶效應,建立長期保護防線。當被病毒感染時將可立即喚起免疫反應
5. 可有效誘導T細胞免疫進而毒殺病毒感染的細胞
6. 為精準設計型次單位疫苗,產生之免疫反應集中
7. 臨床證實為高度安全的疫苗,無論基礎接種或追加劑的應用,皆適用於成年人及年長者等族群之施打
8. UB-612之貯存及運輸僅需在2-8℃之條件即可,大為降低應用成本
